Хронический миелоидный лейкоз (ХМЛ) - хроническое неопластическое заболевание кроветворной системы. Каковы причины и симптомы хронического лейкоцитарного лейкоза? Как проходит лечение? А каков прогноз?
Хронический миелоидный лейкоз (ХМЛ) лейкемический хронический миелоз) составляет около 15 процентов всех лейкозов.
Взрослые страдают им намного чаще, а у детей диагностируют крайне редко.
Пик заболеваемости приходится на возраст от 45 до 55 лет, мужчины болеют хроническим миелоидным лейкозом несколько чаще, чем женщины (1,3: 1). Это злокачественное новообразование, которое встречается у населения с частотой около 1-2 на 100 000 человек в год.
Его характерной особенностью является клональный патологический рост мультипотентных стволовых клеток костного мозга, которые под действием факторов роста трансформируются в клетки гранулоцитарной системы, то есть лейкоциты (белые кровяные тельца).
Стоит отметить, что избыточно продуцируемые гранулоциты у пациентов с ХМЛ функционально эффективны и поддерживают свои функции.
Хронический миелоидный лейкоз: факторы риска ХМЛ
К известным факторам риска развития хронического миелоидного лейкоза относятся воздействие ионизирующего излучения и бензола. Однако в большинстве случаев этиология неизвестна.
Хронический миелолейкоз: причины
В геноме 90-94 процентов людей, страдающих ХМЛ, обнаруживается филадельфийская хромосома (Ph-хромосома), которая является результатом транслокации между хромосомами 9 и 22, t (9,22).
С помощью генетического тестирования можно обнаружить присутствие слитного гена, онкогена BCR-Abl1, который является результатом этой мутации.
Аномальный ген приводит к синтезу дефектного белка с тирозинкиназной активностью. Физиологически он играет важную роль в том, как клетки воспринимают импульсы, которые управляют делением, апоптозом, дифференцировкой и созреванием клеток костного мозга.
Белок bcr-abl, полученный в результате мутации, проявляет постоянную тирозинкиназную активность, что приводит к повышенной и неконтролируемой пролиферации клона миелоидных стволовых клеток.
Хронический миелоидный лейкоз: клинические формы
Есть две формы хронического миелолейкоза. Деление тесно связано с наличием филадельфийской хромосомы в геноме пациентов и ее отсутствием.
Около 90-94% пациентов страдают типичной формой ХМЛ, при которой описана филадельфийская хромосома, в то время как 5% пациентов с атипичным ХМЛ отсутствуют.
У таких пациентов прогноз хуже, поскольку они устойчивы к стандартному фармакологическому лечению.
Хронический миелолейкоз: симптомы
На ранних стадиях хронического миелоидного лейкоза характерных симптомов рака нет. Подавляющее большинство пациентов чувствуют себя хорошо, имеют здоровый аппетит и поддерживают постоянную массу тела.
Заподозрить заболевание на данном этапе развития можно только на основании лабораторных изменений в общем анализе крови (морфологии), поэтому так важно проводить регулярные профилактические осмотры.
В 50% случаев заболевание выявляется во время плановых осмотров, назначенных терапевтом.
На более поздних стадиях хронического миелоидного лейкоза пациенты начинают испытывать менее типичные недуги, которые часто недооценивают, такие как:
- усталость
- потеря веса
- чрезмерное потоотделение
- низкая лихорадка
- боль в костях
- боль в животе
- покалывание в левом подреберье
В таком случае вам следует срочно посетить терапевта, который должен поговорить с пациентом, осмотреть его и, если он сочтет необходимым, заказать лабораторные исследования.
Людей, страдающих заболеваниями кроветворной системы, лечит специалист-гематолог, которому необходимо направление от терапевта.
Симптомы, представленные пациентами на более поздней стадии заболевания, включают:
- непреднамеренная потеря веса за относительно короткий период времени (из-за ускоренного метаболизма)
- отсутствие аппетита
- хроническая усталость, слабость, сонливость, легкая утомляемость, снижение переносимости физических нагрузок
- чрезмерное потоотделение
- лихорадка и субфебрильная температура без видимой причины
- повторяющиеся инфекции
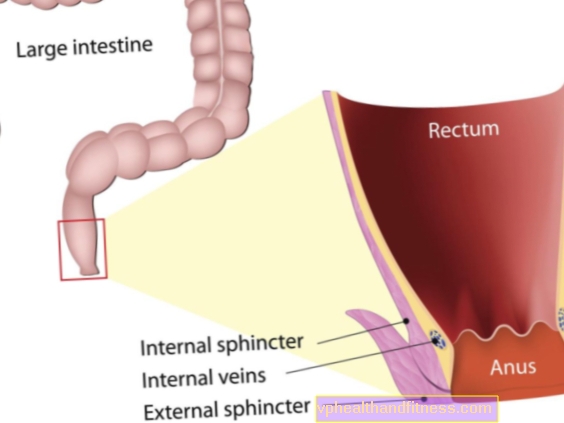
- гепатомегалия, то есть увеличение печени, которое пальпируется при обследовании брюшной полости, проводимом врачом в проекции правого подреберья
- спленомегалия, то есть увеличение селезенки, которое пальпируется при обследовании брюшной полости, проведенном врачом в проекции левого подреберья. Может вызывать колющие боли в левой эпигастральной области. При хроническом миелолейкозе селезенка может достигать очень больших размеров и даже достигать лонного симфиза (физиологически она находится под левым подреберьем, при абдоминальном осмотре не пальпируется)
Хронический миелоидный лейкоз: диагноз
Лабораторные тесты
Среди типичных признаков хронического миелолейкоза, которые описаны в результатах лабораторных исследований.
принадлежат:
- Лейкоцитоз
Характерной особенностью хронического миелолейкоза, на которую сразу обращает внимание врач после получения результатов общего анализа крови (общего анализа крови), является высокий лейкоцитоз, то есть повышенное количество лейкоцитов (лейкоцитов) в периферической крови.
Физиологически количество лейкоцитов должно находиться в пределах 4,0-10,8х109 / л (4,0-10,8 тыс. / Мкл), тогда как у людей с ХМЛ количество лейкоцитов обычно колеблется в пределах 20-50х109. / л (20-50 тыс. / мкл).
Стоит отметить, что ХМЛ - это лейкоз с наибольшим количеством лейкоцитов (даже более 500 000 / мкл)!
Получив такие результаты анализов, семейный врач должен немедленно направить пациента на срочную консультацию к специалисту-гематологу и назначить общий анализ крови с углубленным анализом количества отдельных фракций лейкоцитов (анализ крови с мазком).
Типичным признаком ХМЛ является повышенное количество двух фракций лейкоцитов - базофилов (базофилия) и эозинофилов (эозинофилия).
У пациентов с очень высоким уровнем лейкоцитов и / или тромбоцитов могут возникать симптомы, связанные с лейкостазом и лейкозной эмболией, такие как инсульт, сердечный приступ, нарушения зрения, а также венозный тромбоз.
- Наличие миелобластов в периферической крови
Физиологически бластные клетки присутствуют только в костном мозге и не описаны в периферической крови.
Процент миелобластов - один из критериев, определяющих стадию развития болезни. Присутствие от 10 до 19% миелобластов указывает на фазу обострения болезни, в то время как> 20% информируют врача о бластном кризе.
- Анемия
Нормальное, повышенное или пониженное количество тромбоцитов в зависимости от стадии заболевания.
Повышенная концентрация мочевой кислоты в сыворотке крови - результат усиленного клеточного метаболизма в ходе пролиферативного заболевания.
- Повышенный уровень лактатдегидрогеназы (ЛДГ)
Это результат повышенного клеточного метаболизма в ходе пролиферативного заболевания.
Значительно снижена активность щелочной фосфатазы в лейкоцитах (характерная особенность ХМЛ, при других миелопролиферативных заболеваниях активность этого фермента повышена).
- Фиброз костного мозга
Это случается на более поздней, запущенной стадии болезни.
Исследование костного мозга
Для установления диагноза врач назначает гистопатологическое исследование костного мозга. Чтобы собрать костный мозг для исследования, следует провести тонкоигольную аспирационную биопсию или чрескожную биопсию костного мозга, то есть инвазивные процедуры, проводимые в условиях больницы.
- BAC (тонкоигольная аспирационная биопсия) включает забор костного мозга с помощью специальной иглы со шприцем.
- Чрескожная биопсия костного мозга включает взятие фрагмента кости вместе с костным мозгом с помощью толстой острой иглы после предварительной кожной анестезии.
Чаще всего костный мозг собирают из одной из подвздошных костей (они образуют таз вместе с лобковой, седалищной и крестцовой костями), а точнее - из задней верхней подвздошной ости и грудины.
Методом выбора является тонкоигольная аспирация костного мозга, однако в некоторых случаях этот метод не дает материала для тестирования из-за фиброза костного мозга.
В этом случае следует провести чрескожную биопсию костного мозга.
Результаты исследования костного мозга у пациентов с хроническим миелоидным лейкозом показывают богатое клеточное изображение костного мозга с преобладанием гранулоцитарной системы и наличием повышенного количества гранулоцитопоэтических предшественников («сдвиг влево», то есть появление более молодых форм миелоидных клеток в крови).
Проведение тонкоигольной аспирационной биопсии необходимо в связи с необходимостью оценки процента бластов, что позволяет определить стадию неопластического заболевания, а также провести цитогенетический тест, в ходе которого оценивается кариотип клеток костного мозга.
Цитогенетические и биомолекулярные исследования
Цитогенетический (материал, взятый из костного мозга) и биомолекулярный (материал, собранный из периферической крови) у пациентов с хроническим миелоидным лейкозом считается «золотым стандартом» в диагностике и мониторинге лечения.
Он показывает наличие филадельфийской хромосомы и слитного гена, онкогена BCR-Abl1, который является результатом t-мутации (9,22).
Это имеет ключевое значение не только для определения диагноза рака, метода лечения и его прогноза, но и для мониторинга реакции на терапию.
Лечение хронического миелоидного лейкоза контролируется путем подсчета количества клеток, содержащих филадельфийскую хромосому.
Полным цитогенетическим ответом на лечение считается состояние, при котором в тестируемом материале не обнаруживаются Ph + -клетки, а частичным цитогенетическим ответом - когда количество Ph + -клеток колеблется от 1 до 35%.
Хронический миелоидный лейкоз: клинические фазы типичной формы
Хронический миелолейкоз имеет трехфазное течение. Выделяют 3 стадии развития болезни:
- хроническая фаза (стабильный хронический период)
На этой стадии заболевание обычно носит скрытный характер без типичных клинических симптомов. Пациенты могут заметить усталость, ночную потливость или снижение толерантности к физическим нагрузкам. 85% пациентов диагностируются на этой стадии развития новообразования, что является благоприятным прогнозом. На это уходит в среднем 3-5 лет. - фаза разгона (период разгона)
Этот период заболевания диагностируется при процентном содержании миелобластов в периферической крови по данным ВОЗ составляет от 10 до 19%. У пациентов появляются первые клинические симптомы опухолевого заболевания, такие как увеличение селезенки, лихорадка, лейкоцитоз, анемия и тромбоцитопения. Средняя выживаемость пациентов в этой фазе заболевания составляет 1-2 года. - бластическая фаза (ерш, взрывной кризис)
Третья стадия заболевания характеризуется процентным содержанием миелобластов и промиелоцитов> 20% в периферической крови (ранее использованный критерий был> 30%). Бластный криз протекает тяжело, подобно острому лейкозу, характеризуется устойчивостью к лечению, плохим прогнозом и, как правило, летальным исходом. Средняя выживаемость пациентов составляет 3-6 месяцев. Согласно литературным данным, курение значительно ускоряет наступление бластного криза у людей, страдающих хроническим миелолейкозом!
КРИТЕРИИ ДИАГНОСТИКИ ФАЗЫ УСКОРЕНИЯ И БЛАСТИЧЕСКОГО ПРОРЫВА ХРОНИЧЕСКОЙ ЛЕЕЛОНОМЫ ПО ВСЕМИРНОЙ ОРГАНИЗАЦИИ ЗДРАВООХРАНЕНИЯ (ВОЗ)
КРИТЕРИИ ФАЗЫ УСКОРЕНИЯ (наличие> = 1 симптома)
- Периферическая кровь или бласты костного мозга 10-19%
- базофилия> = 20%
- тромбоцитопения <100000 / мкл
- тромбоцитопения> 1мн / мкл (рефрактерная)
- клональная цитогенетическая эволюция (дополнительные хромосомные аберрации)
- увеличение селезенки или лейкоцитоз, резистентный к лечению
КРИТЕРИИ БЛАСТИЧЕСКОГО РАЗРЫВА (наличие> = 1 симптома)
- процент взрыва> = 20%
- экстрамедуллярные лейкозные инфильтраты
КРИТЕРИИ ДИАГНОСТИКИ ФАЗЫ УСКОРЕНИЯ И БЛАСТИЧЕСКОГО РАЗРЫВА ХРОНИЧЕСКОГО ЛЕЙКЕМИЯ ПО ELN (European Leukemia Net)
КРИТЕРИИ ФАЗЫ УСКОРЕНИЯ
- 15-29% бластов в крови или костном мозге
- 30% бластов и промиелоцитов в крови или костном мозге всего, но <30% только бластов
- процент базофилов в периферической крови или костном мозге> = 20%
- длительная тромбоцитопения <100 г / л, не связанная с терапией
- появление клональной эволюции в Ph (+) клетках
КРИТЕРИИ ВЗРЫВНОЙ ФАЗЫ
- бласты составляют> = 30% лейкоцитов периферической крови или ядерных клеток костного мозга
- экстрамедуллярное распространение взрыва
ОЦЕНКА РИСКА ПРОГРЕССИИ У БОЛЬНЫХ ХРОНИЧЕСКИМ МИЛЕМОНИЕВЫМ КОЖЕЙ
Риск прогрессирования хронического миелоидного лейкоза оценивается с помощью формулы Хасфорда, которая учитывает возраст пациента, размер селезенки ниже реберной дуги, процент базофилов (базофилов), процент эозинофилов и количество тромбоцитов. По результатам выделены три группы пациентов: низкий, средний и высокий риск прогрессирования заболевания.
Хронический миелолейкоз: лечение
Существует несколько методов лечения хронического миелоидного лейкоза, специалист-гематолог решает, какая схема лечения подходит пациенту, учитывая его возраст, состояние здоровья, индекс риска и наличие лекарств. Целью терапии является полное излечение или максимально возможное выживание.
- Трансплантация костного мозга
Чаще всего аллогенную трансплантацию костного мозга проводят после миелоаблативного лечения. Это единственный метод лечения, дающий пациенту шанс на полное выздоровление.
Реципиентам пересаживают костный мозг, взятый от донора того же вида, чаще всего от семьи и родственников. При отсутствии родственников, которые могут сдать костный мозг для трансплантации, возможна и трансплантация от посторонних людей, к сожалению, такого донора найти сложно.
Условием для прохождения аллогенной трансплантации костного мозга является возраст пациента до 55-60 лет. возраст.
В литературе сообщается, что наилучшие результаты в лечении хронического миелоидного лейкоза достигаются, когда трансплантация костного мозга выполняется в первый год болезни, в первой хронической фазе, а донором являются братья и сестры пациента, совместимые с основным комплексом гистосовместимости HLA (Human Leukocyte Antigens). .
Этот метод лечения считается наиболее полезным для пациентов на ранних стадиях ХМЛ.
Вероятность излечения оценивается в 40-70%, когда трансплантация костного мозга проводится в хронической фазе заболевания, 10-30% во время фазы ускорения и менее 10% во время фазы взрыва (тогда это связано с высоким риском смерти).
Стоит отметить, что трансплантация костного мозга сопряжена с рядом осложнений, наиболее частым из которых на практике является болезнь трансплантат против хозяина (GvHD).
Это основная причина смерти людей, получающих лечение этим методом. Показано, что вероятность острой РТПХ у пациентов после трансплантации костного мозга составляет 47%, а у хронических больных - 52%.
- Фармакотерапия
Иматиниб (блокатор тирозинкиназы)
Это препарат выбора для пациентов, которым трансплантация костного мозга по разным причинам невозможна.
Интерферон альфа
Это лекарство, используемое у пациентов с типичной формой хронического миелоидного лейкоза. Было доказано, что у 30% пациентов он вызывает длительный высокий цитогенетический ответ и продлевает жизнь пациентов в среднем на 20 месяцев по сравнению с лечением гидроксикарбамидом. Его часто используют в сочетании с цитарабином или гидроксимочевиной.
Гидроксикарбамид (гидроксикарбамид)
Фармацевтический препарат, применяемый на начальной стадии лечения хронического миелолейкоза, с целью уменьшения массы лейкозных клеток, а также в симптоматическом и паллиативном лечении.Он также используется, когда пациент не подходит для трансплантации костного мозга из-за состояния здоровья, возраста или сопутствующих заболеваний, и не достиг клинического улучшения после лечения интерфероном альфа и иматином.
- Лейкеферез
Лейкаферез - это метод немедленного уменьшения количества лейкоцитов в периферической крови с использованием профессиональных центробежных сепараторов клеток.
Это лечение проводится только в специализированных центрах, которые имеют необходимое оборудование. Он заключается в выполнении двух внутривенных проколов в обоих локтях после предварительной дезинфекции мест инъекций.
Периферическая цельная кровь собирается из вены на одной верхней конечности в сепаратор, где белые кровяные тельца отделяются от других морфотических элементов крови и плазмы.
В конце процедуры кровь, лишенная избыточного количества лейкоцитов, возвращается в кровоток через прокол другой верхней конечности.
Этот метод используется только в исключительных случаях, когда врач хочет избежать специализированного фармакологического лечения, например, во время беременности, а также в случае очень высокого лейкоцитоза, который создает риск лейкозной эмболии.
Однако эта процедура является дорогостоящей и технически сложной и поэтому редко используется на практике.
Хронический миелоидный лейкоз: оценка ремиссии и наблюдение
Не только во время терапии, но и после завершения лечения очень важно оставаться в постоянном контакте с гематологом, проводящим терапию, и выполнять предписанные контрольные обследования.
Это анализы крови, биохимические тесты (для оценки возможной токсичности и воздействия на печень), цитологические и цитогенетические тесты костного мозга, а также молекулярные тесты количества транскрипта BCR / ABL.
Оценка молекулярной ремиссии проводится каждые 3 месяца в первый год лечения, а затем каждые 6 месяцев в последующие годы, пока пациент все еще находится в стадии ремиссии.
Хронический миелоидный лейкоз: дифференциация
Хронический миелолейкоз следует дифференцировать от других форм миелопролиферативных новообразований, с фиброзом костного мозга, лейкозными реакциями, а также с хроническим нейтрофильным лейкозом и хроническим миеломоноцитарным лейкозом. Однако при этих болезненных состояниях филадельфийская хромосома отсутствует!
Хронический миелоидный лейкоз: прогноз
Средняя выживаемость людей с хроническим миелоидным лейкозом составляет примерно 3-6 лет. После трансплантации костного мозга 10-летняя выживаемость наблюдается примерно у 55% пациентов.
30% пациентов, получавших только фармакологическую химиотерапию, живут 5 лет после окончания лечения (средняя продолжительность жизни пациентов, получавших гидроксикарбамид, составляет 3-4 года).
Полное выздоровление возможно только при аллогенной трансплантации костного мозга. Очень важно диагностировать новообразования на ранней стадии и своевременно назначить лечение в специализированном центре.